(S)-isoserin 15a (21 g, 0,20 mol) blev opløst i tetrahydrofuran (100 ml), og et blandet opløsningsmiddel af 10 procent vandig natriumhydroxidopløsning (100 ml), di-tert-butyldicarbonat (50 ml, 0,22 mol) blev tilsat dråbevis. Reaktionen blev udført ved stuetemperatur i 9 timer. Den vandige fase blev justeret til pH 2 med 4 mol/l saltsyre og ekstraheret med dichlormethan/methanol (v/v = 5/1, 50 ml x 3) Filtrer ved sugning, koncentrer under reduceret tryk. Titelforbindelsen 15b blev opnået som en farveløs olie (35 g, udbytte: 85 procent).
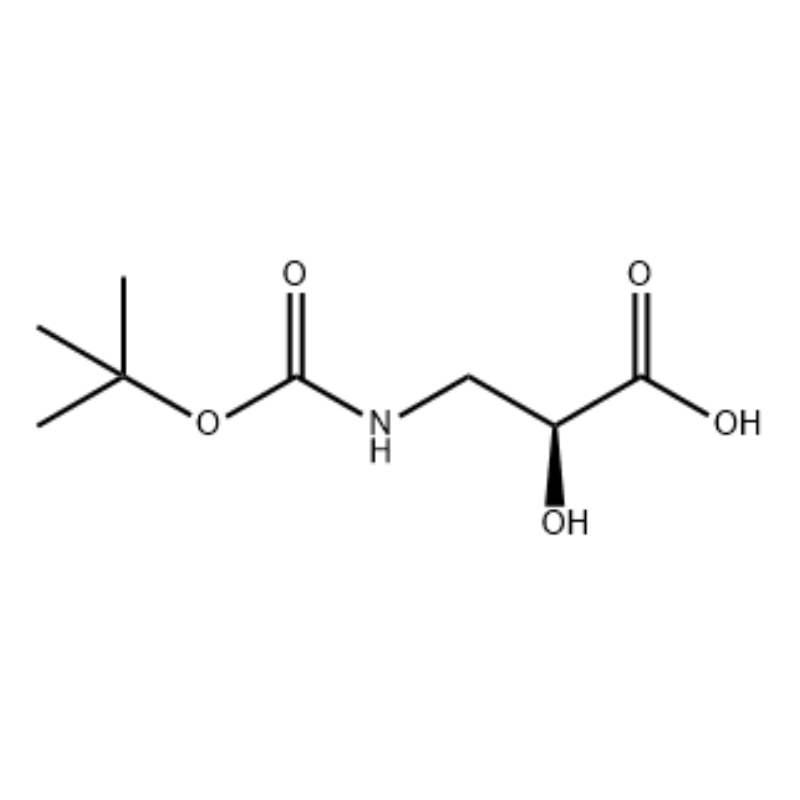
Til en omrørt opløsning af S-isoserin (4,0 g, 0,038 mol) i dioxan: H2O (100 ml, 1:1 v/v) ved 0°C blev tilsat N-methylmorpholin (4,77 ml, 0,043 mol) efterfulgt af BoC2O (11,28 ml, 0,049 mol), og reaktionsblandingen blev omrørt natten over med gradvis opvarmning til stuetemperatur.Glycin (1,0 g, 0,013 mol) blev derefter tilsat, og reaktionsblandingen blev omrørt i 20 min.Reaktionsblandingen blev afkølet til 0°C og mættet vandig.NaHC03 (75 ml) blev tilsat.Det vandige lag blev vasket med ethylacetat (2 x 60 ml) og derefter forsuret til pH 1 med NaHS04.Denne opløsning blev derefter ekstraheret med ethylacetat (3 x 70 ml), og disse kombinerede organiske lag blev tørret over Na2S04, filtreret og koncentreret til tørhed for at give den ønskede N-Boc-3-ammo-2(S)-hydroxypropansyre (6,30 g, 0,031 mmol, 81,5 procent udbytte): 1H NMR (400 MHz, CDC13) 5 7,45 (bs, 1 H), 5,28 (bs, 1 H), 4,26 (m, 1 H), 3,40-3,62 (m 2H, 2,09 (s, 1 H), 1,42 (s, 9 H);13C NMR (IOO MHz, CDC13) 5 174,72, 158,17, 82, 71,85, 44,28, 28,45.
N-Boc-3-amino-2(S)-hydroxy-propionsyre;Til en omrørt opløsning af S-isoserin (4,0 g, 0,038 mol) i dioxan: H2O (100 ml, 1:1 v/v) ved 0°C blev tilsat N-methylmorpholin (4,77 ml, 0,043 mol), efterfulgt af BoC2O (11,28 ml, 0,049 mol), og reaktionsblandingen blev omrørt natten over med gradvis opvarmning til stuetemperatur.Glycin (1,0 g, 0,013 mol) blev derefter tilsat, og reaktionsblandingen blev omrørt i 20 min.Reaktionsblandingen blev afkølet til 0°C og mættet vandig.NaHC03 (75 ml) blev tilsat.Det vandige lag blev vasket med ethylacetat (2 x 60 ml) og derefter forsuret til pH 1 med NaHS04.Denne opløsning blev derefter ekstraheret med ethylacetat (3 x 70 ml), og disse kombinerede organiske lag blev tørret over Na2S04, filtreret og koncentreret til tørhed for at give den ønskede N-Boc-3-amino-2(5)-hydroxypropansyre (6,30 g, 0,031 mmol, 81,5 procent udbytte): 1H NMR (400 MHz, CDC13) 5 7,45 (bs, 1 H), 5,28 (bs, 1 H), 4,26 (m, 1 H), 3,40-3,62 (m 2H, 2,09 (s, 1 H), 1,42 (s, 9 H);13C NMR (100 MHz, CDC13) 5 174,72, 158,17, 82, 71,85, 44,28, 28,45.
 Bygning 12, nr. 309, South 2nd Road, Economic Development Zone, Longquanyi District, Chengdu, Sichuan, Kina.
Bygning 12, nr. 309, South 2nd Road, Economic Development Zone, Longquanyi District, Chengdu, Sichuan, Kina. amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com
amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com +86 (028) 84841969
+86 (028) 84841969 +86 135 5885 5404
+86 135 5885 5404

















.png)


